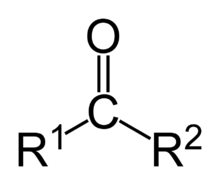
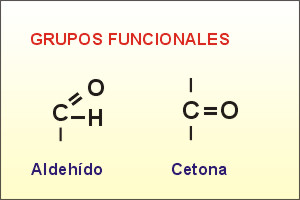
Un éster es un compuesto formado junto con agua por la reacción de un ácido y un alcohol. Puesto que este proceso es análogo a la neutralización de un ácido (R) por una base en la formación de una sal, antiguamente los ésteres eran denominados sales etéreas. Este término es incorrecto porque los ésteres, a diferencia de las sales, no se ionizan en disolución.
En química los ésteres son compuestos orgánicos en los cuales un grupo orgánico reemplaza a un átomo de hidrógeno o más de uno, en un ácido oxigenado. Un ácido oxigenado es un ácido cuyas moléculas poseen un grupo OH– desde el cual el hidrógeno (H) puede disociarse como un ión protón (H+).
Propiedades físicas.- los ésteres pueden participar en los enlaces de hidrógeno como aceptadores, pero no pueden participar como dadores en este tipo de enlaces, a diferencia de los alcoholes de los que derivan. Esta capacidad de participar en los enlaces de hidrógeno les convierte en más hidrosolubles que los hidrocarburos de los que derivan. Pero las ilimitaciones de sus enlaces de hidrógeno los hace más hidrofóbicos que los alcoholes o ácidos de los que derivan. Esta falta de capacidad de actuar como dador de enlace de hidrógeno ocasiona el que no pueda formar enlaces de hidrógeno entre moléculas de ésteres, lo que los hace más volátiles que un ácido o alcohol de similar peso molecular.
Propiedades químicas.-los éteres tienen muy poca reactividad química, debido a la dificultad que presenta la ruptura del enlace C—O. Por ello, se utilizan mucho como disolventes inertes en reacciones orgánicas. En contacto con el aire sufren una lenta oxidación en la que se forman peróxidos muy inestables y poco volátiles. Estos constituyen un peligro cuando se destila un éter, pues se concentran en el residuo y pueden dar lugar a explosiones. Esto se evita guardando el éter con hilo de sodio o añadiendo una pequeña cantidad de un reductor (SO4Fe, LiAIH4) antes de la destilación.
Muchos ésteres tienen un aroma característico, lo que hace que se utilicen ampliamente como sabores y fragancias artificiales. Por ejemplo:
butanoato de metilo: olor a Piña,
octanoato de heptilo: olor a frambuesa
etanoato de pentilo: olor a plátano
pentanoato de pentilo: olor a manzana
butanoato de pentilo: olor a pera o a albaricoque
etanoato de octilo: olor a naranja.
 |
| Grupo funcional éster |
Ejemplos
Salicilato de metilo
El salicilato de metilo ó aceite de bétula ó aceite de gaultería ó aceite de Wintergreen es un líquido incoloro, amarillo o rojizo que tiene el olor y sabor de la gaultería. Comercialmente se emplea en perfumes y como saborizante en caramelos. Se emplea como ingrediente analgésico en linimentos y para contrairritación cutánea ya que al frotarlo en la piel posee la propiedad común de penetrar a través de la superficie. Con esto ocurre la hidrólisis, liberando ácido salicílico, el cual alivia el dolor. Su aplicación excesiva ha producido fallecimientos. Se ha clasificado como veneno pediátrico y debe prescribirse el uso en terapéutica.
Éster fenilmetílico
El benzoato de bencilo (Acido benzoico, éster fenilmetílico) es muy empleado en el tratamiento de la sarna y también es útil en el tratamiento de la pediculosis (afección cutánea producida por piojos). No debe aplicarse sobre piel inflamada, irritada con quemaduras, no debe usarse en mucosas y cara.







.jpg)